化學科學與工程學院陳偉傑課題組通過鈀催化環內1-氮雜烯丙基負離子的芳基化反應實現不對稱合成無保護順式-2,3-二芳基哌啶🥣,相關成果發表於《德國應用化學》
來源:化學科學與工程學院
時間:2023-08-02 瀏覽💔:
3-芳基哌啶結構廣泛存在於具有生物活性的小分子化合物中。已知的合成方法大多需要通過較為繁瑣的步驟構建哌啶環或進行3-位官能團轉化,最終得到氮原子有保護基的三級胺產物。同時,該類化合物的不對稱合成研究較少。因此🚵🏿♀️,發展新的方法由簡單易得的原料便捷地合成3-芳基哌啶類化合物是一個重要研究方向。
近日🕖,我校化學科學與工程學院陳偉傑研究員課題組與美國佛羅裏達大學Daniel Seidel教授合作,基於有機合成中少有研究的環內1-氮雜烯丙基負離子中間體👨🦯,通過鈀催化芳基化反應實現了無保護順式-2,3-二芳基哌啶化合物的快速合成👷🏻♀️🐢,並實現了這一反應的不對稱化🥦。相關成果“Palladium-Catalyzed Arylation of Endocyclic 1-Azaallyl Anions: Concise Synthesis of Unprotected Enantioenriched cis-2,3-Diarylpiperidines”以Communication的形式在線發表於化學領域國際著名學術期刊《德國應用化學》。

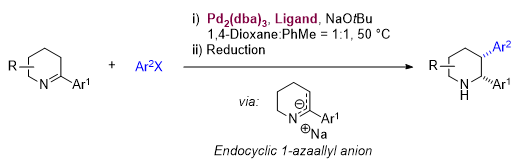
圖1. 鈀催化環內1-氮雜烯丙基負離子的芳基化反應(圖片來源:Angew. Chem. Int. Ed.)
在前期研究基礎上,作者由哌啶出發通過兩步反應合成了底物2-芳基-1-哌啶亞胺🍡。通過叔丁醇鈉去質子化😋,2-芳基-1-哌啶亞胺原位生成相應的環內1-氮雜烯丙基負離子,並在Pd2(dba)3/XPhos催化下與芳基氯發生偶聯反應得到2,3-二芳基-1-哌啶亞胺,隨後通過硼氫化鈉還原以中等至較高的收率和高非對映選擇性得到氮原子無保護的順式2,3-二芳基哌啶♔🥀。該反應適用於烯基氯、含有雜芳基的底物,以及多取代1-哌啶亞胺底物👰🏽。由於環內1-氮雜烯丙基負離子是兩可的親核中間體,對於大多數底物反應還同時得到少量N,3-二芳基化烯胺副產物#️⃣。
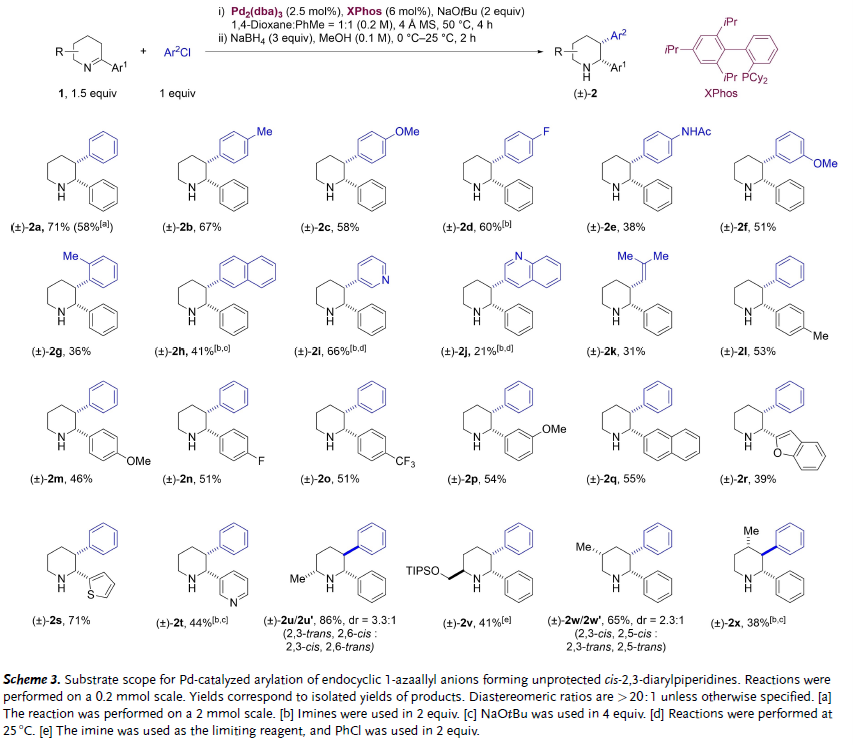
圖2. 消旋反應底物擴展(圖片來源:Angew. Chem. Int. Ed.)
作者進一步利用手性單膦配體實現了該反應的不對稱化🧎🫱🏽。研究發現😈,對於不對稱反應,使用溴苯作為親電芳基化試劑和降低堿的量顯著提高了反應的對映選擇性,同時亞胺當量由1.5倍增加至2倍能夠提高目標產物的收率🧑🏽🏭🧟。大多數底物在Pd2(dba)3/(2R, 3R)-iPr-BI-DIME催化下能夠以中等至較高的收率和對映選擇性得到目標產物。
該方法的最終產物為氮原子無保護的二級胺,因而通過氮原子官能團化或區域選擇性的α’-C–H鍵官能團化,順式-2,3-二芳基哌啶可以便捷地進一步衍生為許多結構復雜的多取代哌啶化合物。
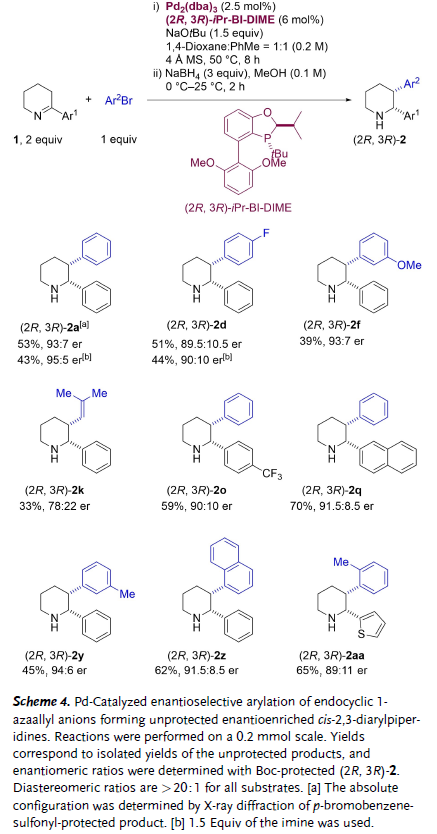
圖3. 鈀催化環內1-氮雜烯丙基負離子的不對稱芳基化反應(圖片來源:Angew. Chem. Int. Ed.)
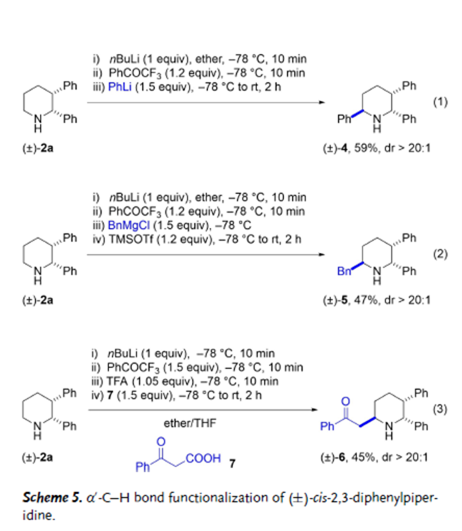
圖4. 無保護順式-2,3-二芳基哌啶的區域選擇性α’-C–H鍵官能團化(圖片來源:Angew. Chem. Int. Ed.)
環內1-氮雜烯丙基負離子由於製備方法的缺乏、結構的不穩定和兩可親核性,此前對其在有機合成中的應用研究很少👩🏽🎤。該工作報道了首例基於環內1-氮雜烯丙基負離子的過渡金屬催化的偶聯反應🗽,極大地擴展了環內1-氮雜烯丙基負離子作為有機合成中間體的價值,實現了由哌啶出發高效對映選擇性地合成無保護多取代哌啶化合物。
陳偉傑研究員為論文第一通訊作者,我校化學科學與工程學院博士生張彪為論文第一作者,恒达平台為論文第一通訊單位🔲。該研究工作得到了國家自然科學基金委✍️、中央高校基本科研業務費以及美國國立衛生研究所資助。
文章鏈接:https://onlinelibrary.wiley.com/doi/10.1002/anie.202307638