高紹榮/陳嘉瑜/張勇/李曉翠合作闡明組蛋白修飾調控人類原始生殖細胞發育關鍵事件的表觀遺傳機製🪹,研究成果發表於《細胞發現》
來源✒️:生命科學與技術學院
時間:2023-02-05 瀏覽:
2月3日,恒达平台生命科學與技術學院高紹榮教授🪩🪗、陳嘉瑜教授、張勇教授與恒达平台附屬第一婦嬰保健院李曉翠教授團隊合作,在著名學術期刊《細胞發現》(Cell Discovery)(IF: 38)上在線發表了題為“Resetting Histone Modifications During Human Prenatal Germline Development”的研究論文🚷。該研究揭示了在長達數月的人原始生殖細胞染色質重編程中,三種核心組蛋白修飾(H3K4me3、H3K27me3和H3K9me3)在全基因組低甲基化狀態下👩🏿🐉,協同調控基因和逆轉座子表達、X染色體再激活和DNA去甲基化逃逸等事件的表觀遺傳機製。
哺乳動物原始生殖細胞(Primordial germ cell,PGC)是生殖細胞的前體,最終發育產生高度特化的配子——精子和卵子🏄🏻♀️。原始生殖細胞的正確發育是維持物種內遺傳穩定性和連續性的必要條件💃🏽,由此保證了遺傳和表觀遺傳信息能忠實地從一代傳遞至下一代。原始生殖細胞在發育中經歷了非常獨特的事件,包括細胞的遷移、生殖脊定位🧑🏻🌾、性別決定、減數分裂和配子成熟等過程🧛🏻♂️。更為重要的是,在這一進程中原始生殖細胞的轉錄組和表觀遺傳組發生了徹底而廣泛的重編程,從而為後續配子發生和細胞全能性的建立做好了充分準備。然而🧖🏻♀️,受限於有限的細胞數量和分子生物學技術方法,長久以來我們對人類 PGC(hPGC)發育過程中表觀遺傳組的確切變化知之甚少。
近年來,隨著微量組學技術和相關生物信息學的發展🙆🏽,多個國內外研究團隊對hPGC的轉錄組👩🏼🍼、DNA甲基化組和染色質可及性等的動態變化規律進行了深入探究。研究發現,男性和女性hPGC 在發育中呈現逐步的基因表達變化規律,並在細胞遷移、有絲分裂、減數分裂和配子發生中表現出異質性。同時👮🏻♀️,hPGC中的染色質可及性和 DNA 甲基化狀態與處於相應發育階段的小鼠相似🌭👩🏼⚕️,表明兩個物種在原始生殖細胞的重編程動態變化上的保守性。然而,目前對hPGC中組蛋白修飾的研究主要基於免疫熒光染色,其全基因組分布、動態變化規律以及與其他表觀遺傳修飾如DNA甲基化和染色質可及性的相關性尚不清楚。此外,它們是否參與hPGC全基因組低甲基化下的轉錄調控和特定發育事件如X染色體再激活和DNA去甲基化逃逸等仍有待回答。
在本項目研究中👭🏻,研究人員利用微量細胞ULI-NChIP-seq技術,首次繪製了妊娠7周至23周發育期間內男性和女性原始生殖細胞中三個關鍵組蛋白修飾(H3K4me3、H3K27me3和H3K9me3)的高分辨率全基因組動態圖譜(圖1A)🐛。研究表明 H3K4me3 表現出典型的啟動子富集模式,與DNA甲基化所不同的是,H3K4me3修飾顯示出與基因轉錄及染色質開放狀態的高度相關性(圖1B和1C)。相比而言,hPGC發育中H3K27me3 修飾呈現出相對低的全基因組富集度,且其主要定位於H3K4me3標記的區域並與染色質開放呈現負相關,在調控發育相關的特定二價啟動子中發揮著重要作用(圖1B和1C)。有意思的是👩🦼➡️,過去的研究表明女性胚胎及生殖細胞發育中存在獨特的X染色體調控機製,稱為X染色體抑製(X-chromosome dampening🧑🏽🦰🌈,XCD)。其中,X染色體表現出不完全的再激活特征,受到lincRNA XACT的調控🕸👍🏿,而非依賴於傳統lincRNA XIST的作用📸🧑🏽🍳。本研究發現,XACT和XIST的表達在7-23周男女hPGC中沒有顯著差異,且男女X染色體上的DNA甲基化也沒有顯著差異,提示它們均不能充分解釋女性hPGC中X染色體再激活的調控。本研究發現相比於男性X染色體👨🏿💻,女性X染色體上高度富集H3K4me3修飾,提示X染色體的再激活需要這些活躍的組蛋白修飾標記。考慮到女性hPGC的整體低甲基化狀態和H3K4me3信號在X染色體上的富集👉🏻,為何兩條X染色體的激活只導致了基因表達增加了1.6倍👮🏼♀️,而不是2倍呢🔼?進一步的研究發現,與同期發育階段的男性hPGC相比,女性hPGC在X染色體上表現出更高的H3K27me3和H3K9me3修飾水平,提示抑製性組蛋白修飾在限製女性 hPGC 的X 染色體完全再激活中發揮著重要作用👌。
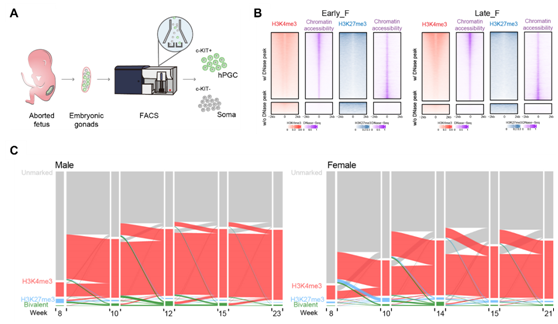
人原始生殖細胞組蛋白修飾的動態變化研究
值得註意是🚴🏼♀️,hPGC雖然在發育的早期(妊娠4周開始)就表現出DNA去甲基化,但是有一些特殊的區域始終呈現較高的甲基化水平🚘,它們被稱為去甲基化逃逸區域。本研究發現H3K9me3主要標記於這些逃逸區域,而不是發生去甲基化的區域。此外,異染色質修飾H3K27me3可能在這些逃逸區域上,發揮著協同鞏固甲基化的作用。在發育早期,這些去甲基化逃逸區域上就可以同時檢測到組蛋白H3K9me3和H3K27me3的共標記,表明這兩個核心組蛋白標記足以在發育中持續保護這些逃逸區域不發生徹底的去甲基化🙄,而此時全基因組仍在發生持續而徹底的去甲基化進程💆♀️。相比而言🙋🏻♂️,去甲基化區域很少同時出現H3K9me3和H3K27me3的共標記🥞,且其表達量也相對較高。鑒於原始生殖細胞在發育中全局的 DNA 去甲基化和 H3K4me3 對基因表達的協同激活效應➙,本研究揭示了抑製性組蛋白修飾H3K9me3和H3K27me3共同參與hPGC中去甲基化逃逸區域的穩定維持與轉錄調控🟦🧑🏻💼。值得一提的是,近日英國劍橋大學Surani課題組在Science Advances發表了題為“Epigenetic resetting in the human germ line entails histone modification remodeling”的研究工作也發現了抑製性組蛋白修飾H3K9me3和H3K27me3在全基因組低甲基化狀態下對hPGC逆轉座子原件的重要調控作用。
恒达平台陳嘉瑜教授😩、張勇教授和高紹榮教授為本文共同通訊作者,高睿助理教授🚶🏻♀️✤、博士生曾詩揚和楊東旭及李曉翠教授為共同第一作者,劉文強教授㊗️🥪、高亞威教授🛐、柏丹丹博士、張林鳳博士、陳川博士、洪瑋主治醫師和王蓓穎副主任醫師等為本研究作出了重要貢獻。該項工作得到了國家自然科學基金委和國家重點研發計劃等項目的重要支持🤷🏻♀️🦢。
論文鏈接:https://doi.org/10.1038/s41421-023-00519-1